| 金刚石、石墨和C60(2) |
主编:黄冈中学化学集体备课组
复习:1、碳的几种单质:金刚石(C)、石墨(C)和C60
(1)金刚石和石墨的性质和用途
金刚石
石墨
外观
无色透明正八面体状晶体,加工琢磨后有夺目光泽
深灰色鳞片状固体,略有金属光泽
导电性
无
良好
硬度
最硬
较软
用途
钻探机钻头、刻刀、装饰品等
电极、铅笔芯、润滑剂等
(2)金刚石和石墨的物理性质有很大差异的原因是:碳原子的排列方式不同。
2、无定形碳:由石墨的微小晶体和少量杂质构成.主要有:焦炭,木炭,活性炭,炭黑等。
木炭
作燃料,冶炼金属,作吸附剂(吸附色素和有异味的物质)
活性炭
吸附能力比木炭强,吸附毒气,制糖工业里脱色制白糖
炭黑
制造墨、油墨、油漆、鞋油和颜料,增加轮胎制品的耐磨性
焦炭
冶炼金属
引入:金刚石(C)、石墨(C)和C60的化学性质怎样?
一、碳的化学性质
单质碳的物理性质各异,而各种单质碳的化学性质却完全相同。
1、可燃性:
充分燃烧(氧气充足),生成CO2:C+O2
CO2
不充分燃烧(氧气不充足),生成CO:2C+O2
2CO
讲解:碳充分燃烧和不充分燃烧时,碳和氧气的质量关系。
2、碳常温下具有稳定性
3、还原性:
C+2CuO
2Cu+CO2↑(置换反应)
应用:冶金工业
现象:黑色粉末变成红色,澄清石灰水变浑浊。
酒精灯加网罩的作用:使火焰集中,提高温度。
举例讲解:氧化还原反应
Fe3O4+2C
3Fe+2CO2↑
2Fe2O3+3C
4Fe+3CO2↑
C+CO2
2CO
C + H2O
H2 + CO
二、氧化还原反应
含氧化合物里的氧被夺去的反应叫做还原反应;物质得到氧的反应叫做氧化反应。
例1、将3g木炭放入盛有6g氧气的密闭容器中燃烧,完全反应后容器内的气体为( )
A.只有CO B.只有CO2
C.CO和CO2 D.CO2和O2
答案:C
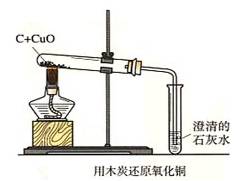
例2、如图是用足量的木炭粉还原氧化铜的装置图,按要求回答:
(1)此实验过程中可观察到哪些现象?____________________
(2)大试管中发生反应的化学方程式为:____________________
(3)试管口要略向下倾斜的原因是______________________________。
(4)实验完毕应进行怎样操作?为什么? ____________________。
(5)实验时,酒精灯加网罩的目的是____________________。
答案:
(1)黑色粉末变成红色,澄清石灰水变浑浊
(2)2CuO+C
2Cu+CO2↑
(3)防止湿存的水倒流引起灼热试管炸裂
(4)先从试管内取出导管,后熄灭酒精灯;防止石灰水倒吸入试管中,使灼热试管破裂
(5)集中火力,提高温度
总结:
一、碳的化学性质:
1、可燃性
2、碳常温下具有稳定性
3、还原性:
二、氧化还原反应
年级 |
课程名称 |
免费听课 |
课程详情 |
| 高一全科点睛班课程 |
|||
| 高一全科强化班课程 | |||
| 高二全科全年强化班 |
|||
| 高三全科强化班课程 |
|||
| 初一全科强化班课程 | |||
| 初一全科点睛班课程 | |||
| 初二全科强化班视频 |
|||
| 初二全科点睛班课程 |
|||
| 初三全科强化班 |
|||
| 全科巨无霸同步提高课程 | |||
| 小学全年全科强化班 |
|||
- 返回 -