| 金属键 |
主编:黄冈中学化学集体备课组
一、金属
1、金属键:
在金属中金属阳离子与自由电子之间的较强作用叫做金属键。
(1)金属键的本质:一种电性引力。
(2)金属键的特点:无方向性,无饱和性。
注意:金属键的特征是成键电子可以在金属中自由流动,金属键是一种遍布整个晶体的离域化学键,使得金属呈现出特有的属性(如导电导热性,延展性等)。
2、金属晶体:
通过金属离子与自由电子之间的较强作用(金属键)形成的单质晶体叫做金属晶体。
要从以下结构方面理解金属晶体:
(1)构成粒子:金属阳离子和自由电子。
注意:在金属晶体里,自由电子不专属于某一个或几个特定离子,它们几乎均匀地分布在整个晶体中,被许多金属离子所共有。“金属离子沉浸在自由电子的海洋里”。
(2)粒子间相互作用:金属键。
(3)金属键的差别很大,使金属的熔沸点,硬度差别也很大。
如:金属钠的熔点较低、硬度较小,而钨是熔点高、硬度大的金属,这是由于形成的金属键强弱不同的缘故。
(4)金属键强弱及其对金属晶体物理性质的影响:金属阳离子半径越小,所带荷电荷数越多,金属键越强,所形成金属的熔沸点越高,硬度越大。
3、电子气理论及其对金属通性的解释
(1)电子气理论
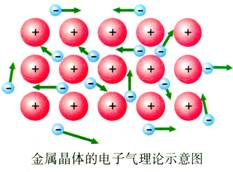
经典的金属键理论叫做“电子气理论”。它把金属键形象地描绘成从金属原子上“脱落”下来的价电子形成遍布整块晶体的带负电的“电子气”,被所有原子所共用,从而把所有金属原子维系在一起。金属原子则“浸泡”在“电子气”的“海洋”之中。由此可见,金属晶体跟原子晶体一样,是一种“巨分子”。
(2)金属通性的解释
思考:
金属有哪些共同的物理性质呢?
金属共同的物理性质:易导电、导热、有延展性、有金属光泽等。
①金属导电性的解释
在金属晶体中,充满着带负电的“电子气”,这些电子气的运动是没有一定方向的,但在外加电场的条件下电子气就会发生定向移动,因而形成电流,所以金属容易导电。
②金属导热性的解释
金属容易导热,是由于电子气中的自由电子在热的作用下与金属原子频繁碰撞从而把能量从温度高的部分传到温度低的部分,从而使整块金属达到相同的温度。
思考:
导热是能量传递的一种形式,它必然是物质运动的结果,那么金属晶体导热过程中电子气中的自由电子担当什么角色?
通过自由电子的热运功传递热量。
③金属延展性的解释
当金属受到外力作用时,晶体中的各原子层就会发生相对滑动,但不会改变原来的排列方式,弥漫在金属原子间的电子气可以起到类似轴承中滚珠之间润滑剂的作用,所以在各原子层之间发生相对滑动以后,仍可保持这种相互作用,因而即使在外力作用下,发生形变也不易断裂。因此,金属都有良好的延展性。
④金属形成合金性能发生改变的解释
当向金属晶体中渗入不同的金属或非金属原子时,就像在滚珠之间渗入了细小而坚硬的砂土或碎石一样,会使这种金属的延展性甚至硬度发生改变,即金属材料形成合金以后性能发生了改变。
二、金属知识拓展
1、超导体――一类急待开发的材料
一般说来,金属是电的良好导体(汞的很差)。 1911年荷兰物理学家H・昂内斯在研究低温条件下汞的导电性能时,发现当温度降到约4 K(即―269°C)时汞的电阻“奇异”般地降为零,表现出超导电性。后又发现还有几种金属也有这种性质,人们将具有超导性的物质叫做超导体。
2、合金
两种和两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质,叫做合金。合金属于混合物,对应的固体为金属晶体。
合金的特点:①仍保留金属的化学性质,但物理性质改变很大;②熔点比各成份金属的都低;③强度、硬度比成分金属大;④有的抗腐蚀能力强;⑤导电性比成分金属差。
3、金属的物理性质
由于金属晶体中存在大量的自由电子和金属离子(或原子)排列很紧密,使金属具有很多共同的性质。
(1)状态:通常情况下,除Hg外都是固体。
(2)金属光泽:多数金属具有光泽。但除Mg、Al、 Cu、Au在粉末状态有光泽外,其他金属在块状时才表现出来。
(3)易导电、导热:由于金属晶体中自由电子的运动,使金属易导电、导热。
(4)延展性:多数金属具有良好的延展性。
(5)熔点及硬度:由金属晶体中金属离子跟自由电子间的作用强弱决定。
4、金属的特性
金属除有共同的物理性质外,还具有各自的特性。
(1)颜色:绝大多数金属都是银白色,有少数金属具有特有的颜色。如Au金黄色,Cu紫红色,Cs银白略带金色。
(2)密度:与原子半径、原子相对质量、晶体质点排列的紧密程度有关。最重的为锇(Os)、铂(Pt),最轻的为锂(Li)。
(3)熔点:最高的为钨(W),最低的为汞(Hg),Cs为28.4℃,Ca为30℃。
(4)硬度:最硬的金属为铬(Cr),最软的金属为铯(Cs),钾 (K)、钠(Na)也较软,可用小刀切割。
(5)导电性:导电性能强的为银(Ag)、金(Au)、铜 (Cu),导电性能差的为汞(Hg)。
(6)延展性:延展性最好的为金(Au)、Al。
三、典型例题
1.金属晶体的形成是因为晶体中存在( )
A、金属离子间的相互作用
B、金属原子间的相互作用
C、金属离子与自由电子间的相互作用
D、金属原子与自由电子间的相互作用
答案:C。
2.金属能导电的原因是( )
A、金属晶体中金属阳离子与自由电子间的相互作用较弱
B、金属晶体中的自由电子在外加电场作用下可发生定向移动
C、金属晶体中的金属阳离子在外加电场作用下可发生定向移动
D、金属晶体在外加电场作用下可失去电子
答案:B。
3、金属键具有的性质是( )
A.饱和性
B.方向性
C.无饱和性和方向性
D.既有饱和性又有方向性
答案:C。
4、下列不属于金属晶体共性的是( )
A.易导电 B.易导热
C.有延展性 D.高熔点
答案:D。
5、下列生活中的问题,不能用金属键知识解释的是( )
A.用铁制品做炊具 B.用金属铝制成导线
C.用铂金做首饰 D.铁易生锈
答案:D。
6、金属晶体具有延展性的原因( )
A.金属键很微弱
B.金属键没有饱和性
C.密堆积层的阳离子容易发生滑动,但不会破坏密堆积的排列方式,也不会破坏金属键
D.金属阳离子之间存在斥力
答案:C。
年级 |
课程名称 |
免费听课 |
课程详情 |
| 高一全科点睛班课程 |
|||
| 高一全科强化班课程 | |||
| 高二全科全年强化班 |
|||
| 高三全科强化班课程 |
|||
| 初一全科强化班课程 | |||
| 初一全科点睛班课程 | |||
| 初二全科强化班视频 |
|||
| 初二全科点睛班课程 |
|||
| 初三全科强化班 |
|||
| 全科巨无霸同步提高课程 | |||
| 小学全年全科强化班 |
|||
- 返回 -