| 铜的电解精炼和电镀 |
主编:黄冈中学化学集体备课组
(讲)今天学习电解原理的又一应用:铜的电解精炼和电镀。
一、铜的电解精炼
(讲)一般火法冶炼得到的粗铜中含有多种杂质(如锌、铁、镍、银、金等),这种粗铜的导电性远不能满足电气工业的要求,如果用以制电线,就会大大降低导线的导电能力,因此必须用电解的方法精炼粗铜。
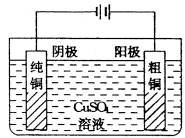
电解时,用粗铜片作阳极,与直流电源的正极相连,用纯铜片作阴极,与电源的负极相连,用CuSO4溶液(加入一定量的硫酸)作电解液。如图:
(讲)电解时,两极发生反应如下:
阳极(粗铜):Cu-2e-=Cu2+
阴极(纯铜):Cu2++2e-=Cu
(讲)可以观察到纯铜变粗,粗铜变细。
(讲)当含杂质的铜在阳极不断溶解时,金属杂质,如Zn、Fe、Ni等,也会同时失去电子,如:
(副版)阳极:Zn-2e-=Zn2+,Fe-2e-=Fe2+,Ni-2e-=Ni2+。
(讲)但是它们的阳离子比Cu2+难以还原,所以它们并不在阴极获得电子析出,因为它们的阳离子得电子能力比Cu2+弱,而只是留在电解液里。而粗铜金属活动性顺序位于铜之后的金、银等杂质,由于失电子能力比铜弱,无法在阳极失电子成为阳离子溶解下来,当阳极上的Cu失去电子变成Cu2+溶解之后,它们便以金属单质的形式沉积在电解槽底,形成了阳极泥(阳极可作为提炼金、银等贵金属的原料),这样在阴极就得到了纯铜。
工业上就是通过以上电解过程来提纯铜的,电解精炼法所得到的铜叫做电解铜,它的纯度很高,可以达到99.95%~99.98%。这种铜的导电性能好,符合电气工业的要求,因此电解铜被广泛用以制作导线和电器等。
(思考)
1、溶液中还有OH-、
等阴离子,阳极为什么不是这些阴离子失电子,而是金属Cu失电子?
答:铜为活泼电级(排在Ag以前的金属电极)比阴离子更容易失电子,所以阳极失电子的不是阴离子,而是金属。
2、电解精炼铜时,电解液中Cu2+浓度是否改变?
答:由于阳极上Cu溶解的速率与阴极上Cu沉积的速率相同,所以溶液中CuSO4浓度基本保持不变,实际略微减小了,因为阳极不仅有Cu失电子,还有Zn、Fe、Ni等杂质失电子,而阴极仅有Cu2+得电子,根据得失中子数相等,但由于所含Fe、Zn、Ni等杂质很少,所以Cu2+基本保持不变,进入溶液中的Cu2+略少于从溶液中析出的Cu2+。若长时间电解,必须补充电解质溶液,还需定时除去其中的杂质离子。
3、电解时,若用粗铜作阴极,纯铜作阳极,结果又会怎样?
答:纯铜溶解,以Cu2+的形式进入溶液,Cu2+在阴极得电子生成Cu附着在粗铜表面,达不到精炼铜的目的。
二、电镀
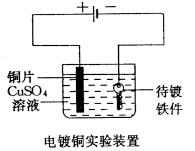
电镀铜实验:
(提问)有何现象?银白色的铁钥匙表面变成紫红色了(附着了一层铜)
分析原因:
阳极:Cu-2e-=Cu2+
阴极:Cu2++2e-=Cu
(讲)像这样利用电解原理在某些金属表面镀上一薄层其它金属或合金的方法叫做电镀。
(板书)
1、电镀:利用电解原理在某些金属表面镀上一薄层其它金属或合金的过程。
(讲)用于电镀的装置,我们叫电镀池,所用的电解质溶液叫电镀液。电镀时,所用的电镀液和浸入电镀液中的电极应满足一定的要求。
2、
(讲)电镀的原理与电解精炼铜的原理一致,无非是将阴极的纯铜换作待镀的金属制品了。
3、电镀的目的
使金属更加美观耐用,增强防锈抗腐能力(因为镀层金属通常是一些在空气或溶液里不易起变化的金属)。
举例:自行车的车把及车圈上镀一层铬后,既美观又耐腐蚀。铁、铝表面镀金、银,不但物美价廉,而且节省资源。其中镀铜是一种应用最广的电镀方法,除了可直接用作金属制品的表层外,通常主要用于电镀其它金属前的预镀层。如在钢铁表面电镀其它金属时,往往要预镀上一薄层镀,然后再镀所需镀的其它金属,这样可使镀层更加牢固和光亮。因此,镀铜是应用最广泛的电镀方法。
练习:用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一种物质(中括号内),溶液能与原来溶液完全一样的是( )
A.CuCl2[CuO] B.NaOH[NaOH]
C.NaCl[HCl] D.CuSO4[Cu(OH)2]
解析:
A.CuCl2
Cu+Cl2↑(补充CuCl2)
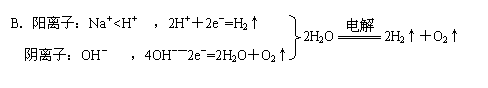
C.2NaCl+2H2O
2NaOH+H2↑+Cl2↑, 2NaOH+2HCl=2NaCl+2H2O
D.CuSO4溶液中:
阴离子:Cu2+>H+,Cu2++2e-=Cu
阳离子:OH->
, 4OH-―4e-=2H2O+O2↑
2CuSO4+2H2O=2Cu+O2↑+2H2SO4
2H2SO4+2Cu(OH)2=2CuSO4+4H2O
答案:C。
总结:
(1)电解不活泼金属无氧酸盐溶液:电解盐本身。
(2)电解含氧酸、强碱、活泼金属含氧酸盐的溶液:实际是电解水。
(3)电解活泼金属无氧酸盐溶液:电解盐和水(显碱色)。
(4)电解不活泼金属含氧酸盐溶液:电解盐和水(显酸性)。
高一全科点睛班课程 高一全科强化班课程 高二全科全年强化班 高三全科强化班课程 初一全科强化班课程 初一全科点睛班课程 初二全科强化班视频 初二全科点睛班课程 初三全科强化班 全科巨无霸同步提高课程 小学全年全科强化班
- 返回 -