1、下列反应不属于可逆反应的是( )
A.工业上利用氮气和氢气合成氨气
B.水电解生成氢气和氧气的混合气体和氢氧混合气体爆炸生成水
C.密闭容器中的二氧化氮和四氧化二氮在一定压力下可以相互转化
D.密闭容器中的二氧化硫和氧气在一定的条件下可以生成三氧化硫,同时三氧化硫又可以分解为二氧化硫和氧气
2、在一密闭容器中充入HI,在一定条件下进行反应:2HI(g)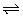 I2(g)+H2(g)。达到平衡状态的标志是( )
I2(g)+H2(g)。达到平衡状态的标志是( )
A.HI的消耗速率是I2的生成速率的2倍
B.单位时问内断裂H―I键的条数等于形成H―H和H―I的条数之和
C.HI和H2的消耗速率之比为2∶1
D.v(H2)正=v(I2)逆
3、可逆反应A(s)+3B(g)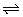 2C(g)+xD(g)在一定温度下进行,下列说法正确的是( )
2C(g)+xD(g)在一定温度下进行,下列说法正确的是( )
A.若x=1,保持容积不变,体系压强也不变时,说明反应已达平衡
B.若x=2,保持容积不变,体系压强也不变时,说明反应已达平衡
C.若x=1,反应在体积可变的衡压容器中进行,容器体积不变时,说明反应已达平衡
D.若x=2,反应在体积可变的衡压容器中进行,容器体积不变时,不能说明反应已达平衡
4、在一定条件下,向5L密闭容器中充入2mol A气体和1mol B气体,发生可逆反应:2A(g)+B(g)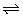 2C(g),达到平衡时容器内B的物质的最浓度为0.1mol・L-1,则A的转化率为( )
2C(g),达到平衡时容器内B的物质的最浓度为0.1mol・L-1,则A的转化率为( )
A.67% B.50%
C.25% D.5%
5、在一定条件下2L密闭容器中加入一定量A发生反应并建立如下平衡:A(g)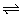 2B(g),2B(g)
2B(g),2B(g)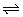 C(g)+2D(g),测得平衡时n(A)=0.3mol,n(B)=0.2mol,n(C)=0.5mol,则最初向容器中加入的A是( )
C(g)+2D(g),测得平衡时n(A)=0.3mol,n(B)=0.2mol,n(C)=0.5mol,则最初向容器中加入的A是( )
A.0.6mol B.0.9mol
C.1.2mol D.1.5mol
6、合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g)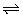 2NH3(g)(正反应为放热反应),673 K、30MPa下,n(NH3)和n(H2)随时间变化关系如图所示,下列说法正确的是( )
2NH3(g)(正反应为放热反应),673 K、30MPa下,n(NH3)和n(H2)随时间变化关系如图所示,下列说法正确的是( )
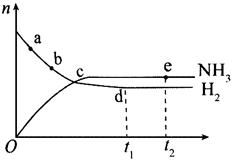
A.c点处正反应速率和逆反应速率相等
B.a点的正反应速率比b点处大
C.d点(t1时刻)和e点(t2时刻)处n(N2)不同
D.t2点时刻,正反应速率大于逆反应速率
7、在密闭容器中进行如下反应:X2(g)+Y2(g)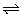 2Z(g)。已知X2、Y2、Z的起始浓度分别为0.1mol・L-1、0.3mol・L-1、0.2mol・L-1,在一定条件下,当反应达到平衡时,各物质的浓度可能是( )
2Z(g)。已知X2、Y2、Z的起始浓度分别为0.1mol・L-1、0.3mol・L-1、0.2mol・L-1,在一定条件下,当反应达到平衡时,各物质的浓度可能是( )
A.Z为0.3mol・L-1
B.Y2为0.35mol・L-1
C.X2为0.2mol・L-1
D.Z为0.4mol・L-1
8、可逆反应:2NO2(g)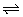 2NO(g)+O2(g),在体积固定的密闭容器中,达到平衡状态的标志是( )
2NO(g)+O2(g),在体积固定的密闭容器中,达到平衡状态的标志是( )
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2、NO、O2表示的反应速率的比为2∶2∶1
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
A.①④⑥⑦ B.②③⑤⑦
C.①⑨④⑤ D.全部
9、Fe(NO3)2溶液呈浅绿色,其中存在下列平衡:Fe2++2H2O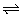 Fe(OH)2+2H+,向该溶液中逐滴加入浓盐酸,发生的变化是( )
Fe(OH)2+2H+,向该溶液中逐滴加入浓盐酸,发生的变化是( )
A.平衡不移动
B.平衡向正反应方向移动
C.溶液颜色由浅绿色变为黄色
D.溶液颜色由浅绿色变为深绿色
10、对于密闭容器中进行的反应:2SO2(g)+O2(g)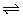 2SO3(g),如果温度保持不变,下列说法正确的是( )
2SO3(g),如果温度保持不变,下列说法正确的是( )
A.增加SO2的浓度,正反应速率先增大,后保持不变
B.增加SO2的浓度,正反应速率逐渐增大
C.增加SO2的浓度,逆反应速率先增大,后保持不变
D.增加SO2的浓度,逆反应速率逐渐增大
11、将2mol水蒸气(H218O)和2mol CO置于1L密闭容器中,在一定条件下,加热至高温,发生如下可逆反应: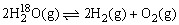 ,2CO(g)+O2(g)
,2CO(g)+O2(g) 2CO2(g)。
2CO2(g)。
(1)平衡后该密闭容器中混合气体的成分共有__________种,其中含18O的物质有__________种。
(2)若平衡时混合气中H2和CO2的物质的量分别a mol和b mol,则O2的物质的量为__________。
12、在体积不变的密闭容器中,保持一定的温度发生下列反应:4A(g)+B(?)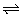 2C(g)+2D(g),请用“增大”“减小”“不变”“能”或“不能”填空。
2C(g)+2D(g),请用“增大”“减小”“不变”“能”或“不能”填空。
(1)当B为固体时,若反应向右进行,容器内混合气体的密度__________,若反应向左进行,容器内混合气体的密度__________,当容器内混合气体的密度不变时,__________说明反应已经达到平衡。
(2)当B为固体时,若反应向右进行,容器内混合气体的平均相对分子质量__________,若反应向左进行,容器内混合气体的平均相对分子质量,当容器内混合气体的平均相对分子质量不变时,__________说明反应已经达到平衡。
(3)当B为气体时,不论向哪个方向反应,容器内混合气体的密度__________,故当容器内混合气体的密度不变时,__________说明反应已经达到平衡。
(4)当B为固体时,不论向哪个方向反应,容器内混合气体的压强__________,故当容器内混合气体的压强不变时,__________说明反应已经达到平衡。
(5)综上可得,若某个量为恒量时,该量不再变化,__________说明反应已经达到平衡;若某个量为变量时,该量不再变化,__________说明反应已经达到平衡。
13、在一定条件下,可逆反应A2(g)+B2(g)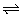 2C(g)达到平衡时,各物质的平衡浓度c(A2)=0.5mol・L-1、c(B2)=0.1mol・L-1、c(C)=1.6mol・L-1,若用a、b、c分别表示A2、B2、C的初始浓度(mol・L-1),则:
2C(g)达到平衡时,各物质的平衡浓度c(A2)=0.5mol・L-1、c(B2)=0.1mol・L-1、c(C)=1.6mol・L-1,若用a、b、c分别表示A2、B2、C的初始浓度(mol・L-1),则:
(1)a、b应满足的关系是______________________________;
(2)a的取值范围是______________________________.
14、(1)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)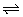 CO2(g)+H2(g)△H<0
CO2(g)+H2(g)△H<0
CO和H2O的浓度变化如图所示,则0~4min的平均反应速率v(CO)=__________mol・L-1・min-1。
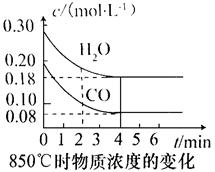
(2)t1℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如下表:
时间/min |
CO/mol・L-1 |
H2O/mol・L-1 |
CO2/mol・L-1 |
H2/mol・L-1 |
0 |
0.200 |
0.300 |
0 |
0 |
2 |
0.138 |
0.238 |
0.062 |
0.062 |
3 |
c1 |
c2 |
c3 |
c3 |
4 |
c1 |
c2 |
c3 |
c3 |
5 |
0.116 |
0.216 |
0.084 |
|
6 |
0.096 |
0.266 |
0.104 |
|
①表中3min~4min之间反应处于__________状态;c1数值__________0.08mol・L-1(填“大于”“小于”或“等于”)。
②反应在4min~5min间,平衡向逆反应方向移动,可能的原因是__________(填字母下同),表中5min~6min之间数值发生变化,可能的原因是__________。
a.增加水蒸气 b.降低温度
c.使用催化剂 d.增加氢气浓度