|
26.(14分)一氧化碳在催化剂作用下能与H2、H2O、烯、炔等反应,是制备有机物的重要原料.工业上将CO和H2的混合气体在一定条件下可合成甲醇.
(1)已知在某温度和压强下:
①2CO(g)+O2(g)═2CO2(g) △H1kJ·mol-1
②2H2(g)+O2(g)═2H2O(g) △H2kJ·mol-1
③2CH3OH(g)+3O2(g)═2CO2(g)+4H2O(g) △H3kJ·mol-1
则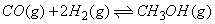 △H=______________________kJ·mol-1 △H=______________________kJ·mol-1
(2)在一定温度下,若将10molCO和20molH2放入2L的密闭容器中,达平衡后测得CO的转化率为40%,则该反应的平衡常数为______________________;若此时再向该容器中投入10molCO、20molH2和10mol CH3OH,判断平衡移动的方向是___________(填“正向移动”、“逆向移动”或“不移动”);新平衡与原平衡相比,CO的物质的量分数___________(填“增大”、“不变”或“减小”).
(3)一定条件下,CO可与粉末状的氢氧化钠作用生成甲酸钠.
①常温时,甲酸的电离平衡常数Ka=1.70×10-4.甲酸钠的水溶液呈碱性,请用离子反应方程式表示其原因_________________,0.1mol/L的甲酸钠溶液pH约为__________(已知:lg17≈1.23, 计算结果保留一位小数)
②向20ml 0.1mol/L的甲酸钠溶液中小心滴加10ml 0.1mol/L的盐酸,混合液呈酸性,请按由大到小的顺序给溶液中离子浓度排序___________________________________________.
|