37、【化学――选修3:物质结构与性质】(15分)
铜是应用较为广泛的有色金属。
(1)基态铜原子的核外电子排布式为__________。
(2)金属化合物Cu2Zn合金能导电,熔点较高、强度、硬度较大。Cu2Zn合金的晶体类型是__________。
(3)某含铜化合物的离子结构如图所示。
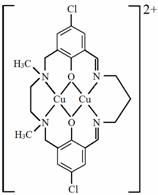
①该离子中存在的作用力有__________;
a.离子键 b.共价键 c.配位键 d.氢键 e.范德华力
②该离子中第二周期的非金属元素的第一电离能由大到小的顺序是__________;
③该离子中N原子的杂化类型有__________。
(4)下图是某铜矿的立方晶胞图,该铜矿用于炼铜时,会产生能使品红溶液褪色的气体,则X的元素符号是__________,此晶胞的化学式__________,与X等距离且最近的X原子个数为__________。
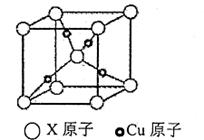
若该晶胞参数为d nm,NA表示阿伏伽德罗常数的值,该晶体的密度为__________g/cm3。
|